發布時間:2019-09-05 發布人:學院辦公室
8月15日,我院病原生物學系楊光教授的研究成果以“The GRA15 protein from Toxoplasma gondii enhances host defense responses by activating the interferon stimulator STING”為題,作為編輯精選文章(Editor Picks)發表于《Journal of biological chemistry》雜志.
地弓形蟲是一種能夠感染所有溫血動物的有核細胞的原蟲。在人類中能夠建立長期慢性感染。全球約有30%的人口既往感染剛地弓形蟲。在免疫缺陷病人中,潛伏感染的剛地弓形蟲重新活化引起危及生命的弓形蟲病。剛地弓形蟲在宿主細胞内繁殖并通過一系列機制調控宿主免疫反應。以往有關識别剛地弓形蟲受體的研究主要集中于Toll樣受體。但細胞質中剛地弓形蟲激活的受體及介導的信号通路仍有待闡釋。
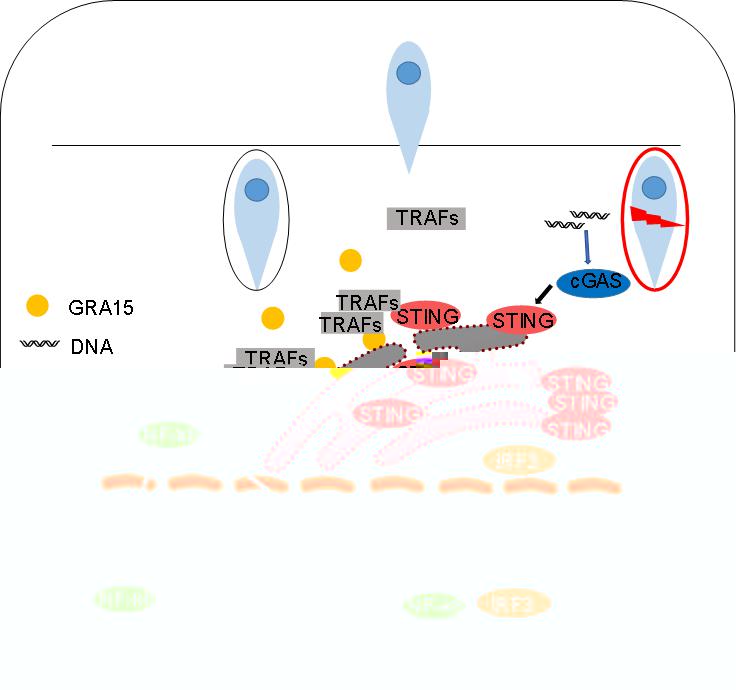
GRA15是一種弓形蟲來源的緻密顆粒蛋白,以往的研究表明,Ⅱ型剛地弓形蟲來源的GRA15依賴TRAF6蛋白激活NF-kB信号通路,進而上調IL-12,IL-1β等細胞因子表達。本研究中,我們發現在小鼠模型中,雙鍊DNA受體cGAS參與抗剛地弓形蟲信号通路。我們還發現與野生型小鼠相比,STING敲除小鼠對剛地弓形蟲更加易感。相應地,感染剛地弓形蟲後,STING敲除小鼠的脾中不能有效表達炎症因子、Ⅰ型幹擾素和幹擾素刺激基因。與cGAS敲除小鼠相比,STING敲除小鼠感染剛地弓形蟲後症狀更嚴重。我們發現,剛地弓形蟲來源的緻密顆粒蛋白GRA15被分泌到宿主細胞質并通過第二跨膜區定位于内質網,進而激活STING從而激活天然免疫反應。進一步的機制研究表明,GRA15依賴TRAF蛋白促進了STING第337位賴氨酸的多聚泛素化和STING的寡聚化。相應地,與野生型剛地弓形蟲相比,GRA15敲除的剛地弓形蟲不能有效激活強烈的天然免疫反應。因此,GRA15缺失的剛地弓形蟲毒性更強,感染野生型小鼠後小鼠死亡率更高。總之,剛地弓形蟲感染激活cGAS/STING信号通路,GRA15依賴STING和TRAF蛋白增強該通路活性(圖1)。
本研究被選為“Editors’ Picks”研究,是在每年6000多篇的JBC發表的文章中精選的前2%。(Our editorial board members and associate editors have determined your paper is in the top 2 percent of manuscripts they will review in a year in significance and overall importance. About 50 to 100 papers are selected from the more than 6,600 we publish each year.)
文章的通訊作者為我院病原生物學系楊光教授和我校講座教授北京大學遊富平研究員。我院為共同通訊作者單位。
文章鍊接:https://www.ncbi.nlm.nih.gov/pubmed/31416833
(基礎醫學院)